Scopo della convalida e della tracciabilità
Lo scopo della convalida è garantire la coerenza di un processo o un sistema e assicurarsi che sia documentato. La convalida del sistema è un requisito delle agenzie di regolamentazione. Per le organizzazioni del settore delle scienze biologiche negli Stati Uniti, ad esempio, tra le agenzie di regolamentazione è inclusa la Food and Drug Administration (FDA).
La FDA definisce la convalida nel seguente modo:
Verifica mediante esame e produzione di prove oggettive che dimostrino che i requisiti particolari per un uso specifico previsto possano essere costantemente soddisfatti.
L'Organizzazione Mondiale della Sanità (OMS) definisce la convalida come segue nelle sue indicazioni sui requisiti per le buone pratiche di fabbricazione:
Produzione di prove documentali che forniscano un elevato grado di garanzia che un processo pianificato sarà uniformemente conforme ai risultati specificati attesi.
Queste definizioni hanno in comune i seguenti elementi, in base ai risultati attesi:
- Produzione di prove
- Conformità alle normative
- Rispetto di requisiti
La convalida dei sistemi computerizzati è un processo documentato per garantire che il sistema faccia esattamente ciò per cui è stato progettato in modo coerente e riproducibile. La convalida garantisce l'integrità e la sicurezza dell'elaborazione dei dati, la qualità del prodotto e la conformità alle normative che si applicano alla buona pratica di {industry} (GxP).
Il processo di convalida di un sistema computerizzato è descritto nelle procedure operative standard e nelle linee guida create e definite dal settore regolamentato, come le organizzazioni di scienze biologiche. Per la convalida dei sistemi computerizzati, è utile vedere l'implementazione del processo come un progetto, come descritto in Buone pratiche di produzione automatizzata (GAMP) 5: un approccio basato sul rischio ai sistemi computerizzati per GxP conformi della International Society for Pharmaceutical Engineering (ISPE).
Prima di iniziare il progetto di implementazione, si dovrebbe creare un piano generale per la nuova soluzione. Si avvia quindi il progetto completando le fasi seguenti:
- Pianificazione: in questa fase, i requisiti e le specifiche sono sufficientemente chiari per una valutazione iniziale del rischio e, in ultima analisi, per una corretta definizione dei test di verifica (protocolli). Durante questa fase, si fornisce il documento del piano di convalida che definisce l'intera strategia di convalida e tutti i risultati finali. La strategia deve essere conforme ai criteri e al sistema di gestione della qualità.
- Specifica, configurazione e codifica: in questa fase vengono realizzate tutte le specifiche di progettazione con il livello di dettaglio richiesto dal tipo di sistema e dal suo utilizzo. Gli sviluppatori scelgono e utilizzano i metodi e gli oggetti di sviluppo più appropriati ai requisiti di codifica e di configurazione e in base alle specifiche approvate. Tutte queste attività vengono svolte nell'ambiente di sviluppo. Durante questa fase, il test è più rivolto alla verifica delle unità o delle funzionalità dal punto di vista dello sviluppatore. Esempi di attività di test includono unit test, test statistici del codice e test di integrazione. Gli strumenti possono automatizzare queste attività di test.
- Test: questa fase conferma che le specifiche sono state rispettate attraverso ispezioni e test del sistema. Le attività di test vengono svolte in un ambiente di test preparato e idoneo. L'ambiente di test deve essere simile all'ambiente di produzione per garantire che le condizioni siano le stesse e per evitare di dover ripetere i test nell'ambiente di produzione. Il rischio deve guidare l'ambito delle attività di test. L'analisi dei rischi può aiutare a comprendere i potenziali pericoli che possono avere un impatto sulla qualità del prodotto, sulla sicurezza del paziente o sull'integrità dei dati. Questi potenziali pericoli devono essere mitigati attraverso i controlli in vigore e i modelli di test. Se c'è un rischio elevato in qualche punto del sistema, con gli scenari di test appropriati si può dimostrare che la progettazione della soluzione è priva di potenziali errori.
- Report e rilascio: in questa fase, il sistema deve essere accettabile per l'uso nell'ambiente di produzione in base a un processo documentato e controllato. Alla chiusura del progetto deve essere predisposto il completamento della convalida del sistema, che riepiloga le attività intraprese e gli eventuali scostamenti dal piano di convalida. La convalida del sistema deve essere completata prima che il sistema venga rilasciato per l'uso.
L'illustrazione seguente mostra il modello a V supportato da GAMP 5, 2a edizione. L'illustrazione fornisce una valida panoramica delle fasi del progetto.
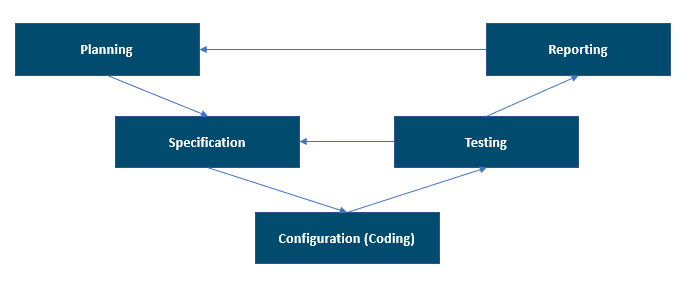
Il modello a V include non solo le attività di sviluppo e i test del sistema, ma anche la loro sequenza, le loro interrelazioni e il processo di convalida dei risultati finali applicabili al sistema computerizzato convalidato. È necessario mantenere e gestire le interrelazioni tra requisiti, specifiche e test. Queste interrelazioni sono documentate nella matrice di tracciabilità che viene utilizzata nelle aree regolamentate.
La matrice di tracciabilità garantisce che:
- I requisiti sono soddisfatti dalla progettazione della soluzione. In altre parole, ogni requisito viene ricondotto alle funzioni, ai controlli, alle configurazioni o agli elementi di progettazione.
- I requisiti vengono testati o verificati per dimostrare che la progettazione della soluzione li rispetta nel modo adeguato.
La matrice di tracciabilità presenta i vantaggi seguenti:
- Supporta la revisione del progetto.
- Aiuta a definire l'ambito dei test di regressione.
- Fornisce supporto durante le attività di ispezione o controllo.
- Fornisce supporto per potenziali modifiche.
Qualifica della piattaforma
I settori regolamentati devono qualificare Microsoft Power Platform come infrastruttura prima di implementare Guides. La qualifica della piattaforma richiede che vengano eseguite almeno le attività seguenti:
Valutazione iniziale del rischio (valutazione dell'applicabilità della GxP)
Valutazione del fornitore (controllo di un fornitore: può essere virtuale, fisico o postale)
Piano di qualifica
Specifica tecnica di progettazione della piattaforma
Valutazione del rischio, ad esempio valutazione del rischio di mettere a disposizione degli operatori la versione sbagliata di una guida
Test:
- Test di installazione, ad esempio i test per verificare che gli ambienti siano installati correttamente
- Test operativi, ad esempio i test per verificare che gli utenti giusti abbiano gli accessi corretti
Report di riepilogo della qualifica
Manuale operativo e della piattaforma e materiali per la formazione
Convalide delle applicazioni
Le applicazioni (come Guides e Power Apps) che supportano i processi aziendali nei settori regolamentati devono essere convalidate. Pertanto, la tua organizzazione deve completare le attività seguenti:
Valutazione iniziale del rischio
Piano di convalida
Requisiti dell'utente
Valutazione del rischio
Specifica funzionale dell'applicazione o specifica tecnica della configurazione
Test (qualifica dell'installazione [IQ], qualifica operativa [OQ] e test di accettazione utente [UAT]):
- Test operativi, ad esempio la verifica di una funzione
- UAT
Matrice di tracciabilità
Report di riepilogo della convalida
Manuale operativo o dell'applicazione e materiali per la formazione